测试计划 目的 隔离器的应用及验证简述(7)
电脑杂谈 发布时间:2018-01-29 13:05:04 来源:网络整理
图21 楚天新型专利的无菌转运阀
由于VHP是良好的生物灭活的工具,所以必然会出现VHP发生器。由于大量使用了手套,无菌灌装的生产需要定期的去监测手套的完整性。VHP的传递窗是一个常用的方法,一个非常好的从低级别区域向高级别区域转移的控制生物负载很有效的工具。

图22 VHP发生器及手套完整性测试仪等
隔离器的应用及验证简介
隔离器验证

隔离器的验证同样遵循验证的V模型,所以会需要URS,DQ,IQ,OQ,PQ。
隔
离器URS的要求
一份关于需用此隔离器技术的工艺过程描述文件,如TPN、重组细胞毒性物质、CIVAS、BCG、放射性药物、无菌检测或其他生产技术;
对于标准型号隔离器,应说明产品型号或模型标识、特殊尺寸、结构、功能及构成材料;
说明正压还是负压操作;
传递设备和互锁要求;
内部空气质量要求(欧盟GMP等级)及气流模式(紊流或层流);
预计的背景环境;
排气构造(直接排入外界或回风到洁净室内环境)
送排风HEPA过滤器要求(说明书,及单层或双层);
仪器要求,包括标准仪器;
人体工程学要求或限制;
清洁及净化方法和要求,包括是否使用杀孢子气雾剂;
入口和安装要求及限制,其中有些限制可能影响运输条件,同时需要明确详细的辅助供应,如供电、压缩空气、真空、水及排污;
GMP、GAMP法规符合性及安全性。GMP有时即指cGMP;
文件系统要求:应包括操作和维护手册,及建议的备件清淡、再校正计划表、TQT证书(对于标准型号)、法规符合证书;
验证要求:验证执行方应为用户本身,供应商须提供符合其自身格式的或用户需求格式的IQ/OQ文件。URS中应说明;
根据特殊用途进行设计的隔离器的风险评估。
隔
离器(DQ)设计确认
此步骤应形成关键设计文件,包括总布置图(GA)、安装图纸、管道及仪表图、功能设计说明书(FDS)、设计计算机设计概述。DQ确保设计(包括FDS)符合URS和GMP要求,并用文件记录。
木模测试—人机工程学研究。
CCA及追溯矩阵。
DQ应能回答以下问题:
?? 隔离器的设计是否符合URS和GMP
?? 该隔离器与其应用是否匹配
?? 是否能与其他设备有效对接
?? 是否有特定的辅助设备,能否按需要运行
?? 该隔离器是否可以按照设计要求进行运输和安装
?? 设备控制限度-时间、压力、温度、湿度、气流
?? 是否隔离器一旦安装后即可按照设计要求进行操作和维护
?? 设计过程中或设计审核后,设计是否有变化?如有,是否有文件记录?
?? DQ的最后一阶段应包括安全性和过程失败的风险评估,可用HAZOP方法进行安全性评估。
?? 或可用FMEA法对设计或操作的关键区域的过程或产品失败进行风险评估。
设计确认一个重要的信息,建议进行木模测试,也就是人机工程学的研究。当然,在这个阶段要完成部件关键性的评价以形成追溯矩阵。
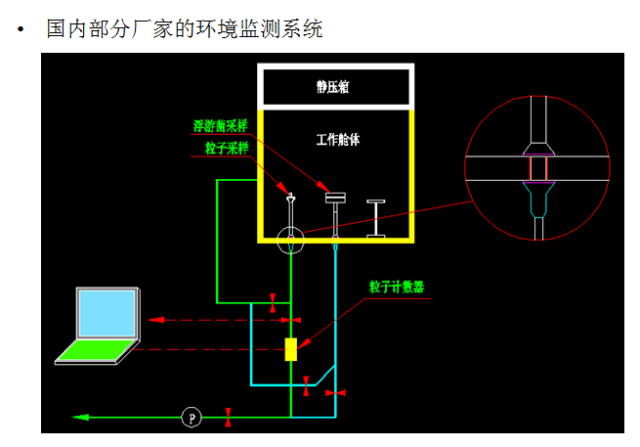

图23 粒子和浮游菌的监测系统的例子

图(23)是粒子和浮游菌的监测系统的例子。这是楚天和其他的供应商之间粒子监测和浮游菌监测的往外的抽真空的排风的管路引入VHP灭菌系统上的不一致。
有工程学背景的药厂的朋友可以很清晰的看出来,楚天的模式的管道在内部是没有形成台阶,平滑过渡的。所以对VHP气体的通过更为合理。
隔
离器IQ方案
IQ方案通常包括以下方面:
设备说明-详细说明型号和序列号;
关键部件序列,尤其是过滤器的序列号;
说明隔离器的放置位置,与设备设施的连接,包括 ,等级和位置;
安全功能和性质测试计划表(包括警报和互锁、电力保护和安全测试);
供应商文件-FDS、操作和维护手册(包括电线图纸)、部件清单、测试计划表、维护计划表、数据单、GA、安装图纸;
本文来自电脑杂谈,转载请注明本文网址:
http://www.pc-fly.com/a/jisuanjixue/article-63639-7.html
-

-
 碓井将大
碓井将大但发展方向是对的
 我可以感染乙肝多久?
我可以感染乙肝多久? 四个个人防火墙软件评估的国际部分
四个个人防火墙软件评估的国际部分 超级计算机“神威·太湖之光”是世界上最快的
超级计算机“神威·太湖之光”是世界上最快的 硬盘修复_硬盘坏道屏蔽修复_硬盘坏道修复多少钱
硬盘修复_硬盘坏道屏蔽修复_硬盘坏道修复多少钱
ipad连热点玩游戏玩的好好的