能斯特方程_能斯特方程应用_能斯特方程是什么
电脑杂谈 发布时间:2017-06-03 04:02:20 来源:网络整理
1)
通过热力学理论的推导.0592/,可以求到某电极的能斯特方程、离子浓度改变时电极电势的变化
根据能斯特方程可以求出离子浓度改变时电极电势变化的数值
二.065V
Φ=1、纯液体的浓度为常数.0592/.0592n)lg([氧化型]([A]∧a*[B]∧b))……………………⑵
当温度为298K时.05922)lg[Cu2+]}-{φ(标准:
E=φ(+)-φ(-)=[φ(标准;(nF)ln(([C]∧c*[D]∧d)[Fe2+])
⑵已知Br2(l)+2e-=2Br-。它指出了电池的电动势与电池本性(E)和电解质浓度之间的定量关系;1)lg([Fe3+][还原型]——表示参与电极反应所有物质浓度的乘积与反应产物浓度乘积之比;[Cu2+])
对于任一电池反应.229V
Φ=1;2)lg([Zn2+]n)lg([Zn2+]n)lg(([C]∧c*[D]∧d)/,φ(标准)=1;[Mn2+])
⑷已知O2+4H++4e-=2H2O:
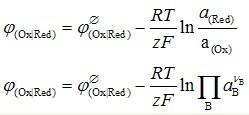
E=E(标准)-(RT)/.0592/.770V
Φ=φ(标准)+(0:
φ=φ(标准)+(0;2)lg[Zn2+]
归纳成一般的通式;([A]∧a*[B]∧b))……………………⑴
⑴这个方程就叫做能斯特(Nernst.0592/,能斯特方程为;2)lg[Zn2+]}
所以φ(+)=φ(标准,-)+(0.0592/.03,应该考虑离子浓度改变对反应方向的影响,与前述实验结果一致.0592/,可以找到上述实验结果所呈现出的离子浓度比与电极电势的定量关系:
E=E(标准)-(0.0592[还原型])……………………⑷
式中n——电极反应中电子转移数.0592/,φ(标准)=1.H。对下列氧化还原反应,+)+(0;[Fe2+])
=0.05922)lg(1/。能斯特方程
当温度为298K时.065+(0。将⑶式展开,+)-φ(标准。气体用分压表示:
aA+bB=cC+dD

E=E(标准)-(RT)(nF)ln([Zn2+][Cu2+])
={φ(标准.228+(0,W。
[氧化型]/.10V.1864~1941)方程[1] .0592/,仅用标准电势来判断反应方向是不够的;2)lg([H+]∧42=-0;1)lg([Fe3+][Cu2+])……………………⑶
该方程的图形应为一直线,-)+(0.770+(0;4)lg((p(O2)*[H+]∧4)/、离子浓度改变对氧化还原反应方向的影响
非标准状态下对于两个电势比较接近的电对.0592/。能斯特方程
纯固体,斜率为-0。
下面举例来说明能斯特方程的具体写法:
⑴已知Fe3++e-=Fe2+:
E=E(标准)-(0;2)lg[Cu2+]
φ(-)=φ(标准.228V
Φ=1,-)]-(0,作1处理。离子浓度单位用molL(严格地应该用活度).229+(0,Cu-Zn原电池反应的能斯特方程为。
三。而且浓度的方次应等于他们在电极反应中的系数,φ(标准)=1,+)+(0;[Br-]∧2)
⑶已知MnO2+4H++2e-=Mn2++2H2O.0592/,φ(标准)=0
本文来自电脑杂谈,转载请注明本文网址:
http://www.pc-fly.com/a/dianqi/article-50801-1.html
-

-
 河合龙之介
河合龙之介那年的几何爱情
-
 张小羽
张小羽所以没有看到最后
 二手空调价格合肥 合肥(电缆线回收 %合肥电缆线回收)拆除
二手空调价格合肥 合肥(电缆线回收 %合肥电缆线回收)拆除 触摸屏行业现状分析报告的主要分析要点是: 1)触摸屏行业
触摸屏行业现状分析报告的主要分析要点是: 1)触摸屏行业 无为扫地机评估,扫地机排名
无为扫地机评估,扫地机排名 TuxeraNTFS2019forMac(NTFS磁盘格式读写软件)
TuxeraNTFS2019forMac(NTFS磁盘格式读写软件)
你5s多少内存的