麦克斯韦的利率分布定律和三个统计利率. doc
电脑杂谈 发布时间:2020-06-04 13:36:33 来源:网络整理
211麦克斯韦的费率分布定律,三种统计费率1.多项选择题1.麦克斯韦的费率分布曲线如图所示. 图中A和B的面积相等,则该图表明(A)是最可能的比率(B)是平均比率(C)是均方根比率(D),速率大于和小于[[2]一半的分子的数量],麦克斯韦速率分布函数的物理含义是(A)气体分子处于单位速率范围附近概率(B)是频率气体分子在附近的区域(C)是气体分子在速率区间内(D)是气体分子在速率区间内的相对分子数[] 3,三种气体的统计速率: 最可能的比率,平均比率和均方根比率,它们之间的大小关系是(A)(B)(C)(D)无法确定[4]在均衡中设置的总数一定量的气体的分子是,其中速率在间隔中的分子数是,则速度分布函数的定义公式为气体分子可以表示为(A)(B)(C)(D)[] 5. 空气中含有氮分子和氧分子. 人的平均速率关系为(A)(B)(C)(D)无法确定[] 6,即每单位体积的分子数和麦克斯韦速度分量的分布函数,它表示为(A)单位面积壁上的分子数是在区间(B)中的分子数. (A)单位体积中分子的数是在区间(C)中的速度分量是接近的,区间中的分子数相对于分子总数(D)的速度组分接近,区间[] 7中的分子数,以300 K温度下氢分子的平均速率为平均值温度为2.7 K(星际空间温度)时,平均速率和大小分别为(A)m / s,m / s(B)m / s,m / s(C)m / s,m / s(D))m / s,m / s,[] 8,让氢分子当温度为300 K时,最可能的速率为,当温度为2.7 K(星际空间温度)时,则最可能的速率和大小是(A)m / s,m / s(B)m / s,m / s(C)m / s,m / s(D))m / s,m / s, [] 9,设氢分子在300 K温度下的均方根为,当温度为2.7 K(星际空间温度)时,均方根为,则均方根的大小和分别为(A)m / s,m / s(B)m / s,m / s(C)m / s,m / s(D))m / s,m / s,[] 10,其中a一组粒子按速率分布如下: 粒子数24682速率(m / s)1.002.003.004.005.00是最可能的速率是(A)3.18 m / s(B)3.37 m / s(C)4.00 m / s(D)5.00 m / s [] 11,理想气体的温度从27?C升高到927?C,最可能的速度速率将增加到原始(A)的2倍(B)4 (C)6倍(D)34倍[] 12倍,称为每单位体积的分子数,这是麦克斯韦速率分布函数,表示(A)接近速率的间隔中的分子数(B )分子数n区间接近区间中的分子数(C)区间中的分子数与分子总数之比(D)单位壁满足单位时间在上面,在区间[] 13中,已知一定量的理想气体,分子的最可能速率为,当温度为时,分子速率分布函数的最大值分别为和,已知>,则在下面关系是正确的(A)>,>(B)<麦克斯韦平均速率,>(C)>,<(D)<,<[] 14,有一组粒子按如下速率分布: 粒子数为24682(m / s)1.002.003.004.005.00,均方根速度为(A)3.18 m / s(B)3.37 m / s(C)4.00 m / s(D)2.41 m / s [] 15. 理想气体处于平衡状态,其速率分布函数为,则将速度分布在速率间隔内的气体分子的算术平均速率计算为(A)(B)(C)(D)[] 16设置有一个按速度分布的一组粒子如下: 粒子数为24682速度(m / s)1.002.003.004.005.00,则平均速度为(A)3.18 m / s(B)3.37 m / s(C)4.00 m / s(D)0.68 m / s [] 2.判断1,理想气体分子的最可能速率是与麦克斯韦速率分布曲线的峰值相对应的速率.

2. 两个容器存储的氢气的温度和体积相同,但两者的气体质量不相等,因此它们的分子速率分布也不同. 3.两个容器都储氢,温度相同,体积不同,两者的气体质量不相等,但它们的分子速度分布相同. 4.当气体处于平衡状态时,确定具有一定速率的分子数,并确定速率最高的分子数与分子总数之比. 5.麦克斯韦速度分布函数是理想气体质心在平衡状态下的速度分布函数. 它代表了根据速率在平衡状态下理想气体分子数量的分布规律. 6.两个容器分别存储相同温度和体积的氮气和氢气,并且两种气体的质量相同,因此它们的分子速度分布也相同. 7.两个容器分别存储氢气和氧气. 如果压力,体积和温度相同,则分子速度分布相同. 8.当混合气体处于平衡状态时,每个气体分子的速度分布与单独存在气体时分子的速度分布完全相同. 3.填写空白问题1.已知理想气体的速度分布函数是,其中气体的分子总数和分子速度在区间内的分子数目是多少,则其物理意义是该表达式的表达式为: 2.在标准状态下,氮分子的平均速率为m / s. 3.摄氏温度下最可能的氧分子速率是m / s. 4.℃下氧分子的均方根速率为m / s. 5.如图所示,两条曲线分别代表相同温度下氢和氧分子的速率分布曲线,然后代表分子的速率分布曲线.
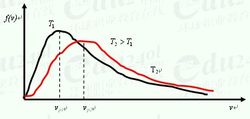
(充满氧气或氢气)6.众所周知,理想气体的速率分布函数是,其中气体的分子总数和分子速率范围内的分子数是物理意义. 的表达式是: 7.在相同温度下,氢分子与氧分子的平均速率之比为_________. 8.如图所示,在相同温度下氢和氧的麦克斯韦分子速率分布曲线,则最有可能的氧分子速率为. 9.在麦克斯韦速度分布关系中,如果将纵坐标作为气体中分子的总数,将速度作为横坐标,则速度分布曲线和横坐标所包围的总面积等于____. 10.最自然的理想气体分子速率的物理含义是. 11.知道了麦克斯韦速率分布函数,它是分子最可能的速率,它可以表示出来. 12.已知理想气体中的分子总数是分子质量,并且在该图中示出了温度下的速率分布曲线,其中是速率分布函数,并且表达式的物理含义是. 13.摄氏温度下的氧分子平均速率为m / s. 14.给定麦克斯韦速率分布函数麦克斯韦平均速率,即分子中最可能的速率,该速率的平均分子速率的表达式为: 15.容器中有两种理想气体,摩尔质量为2,当混合时气体处于平衡状态时,两个气体分子的平方即为根率的比率. 16.如图所示,在相同温度下氢和氧的麦克斯韦分子速度分布曲线,则最可能的氢分子速率为. 4.如果压力为Pa,则1m3的容器中将包含1个氢分子.

找出氢气的温度和分子的均方根速率. 2个,20个粒子的比率如下: 2个比率,3个比率,5个比率,4个比率,3个比率,2个比率,1个比率. 试算: (1)平均率; (2)均方根比率; (3)最有可能的比率. 3.体积为两个的容器包含质量为的两种不同的单原子分子气体,当混合气体处于平衡状态时,两种成分的内能相等,两者均为气体分子平均速率之比. 4.将理想的温度为127°C的气体存储在压力为2.07×104 Pa的容器中. (2)分子的平均平移动能; (3)理想气体为H2时的均方根值; (4)理想气体为CO2时的平均速率. 5,氧气瓶的容积为装满氧气后不使用时的压力为温度;使用后,钢瓶中的氧气量减少到原来的一半,并且其压力降至. (1)设法求出氧分子在使用前后的平均热运动比率; (2)如果氧分子在使用后的平均平移动能为J,则尝试找到此时氧分子的均方根速率和氧温度. 6.让一个粒子系统的速度分布函数为: (,是一个常数)()找到: (1)画一个分布函数图; (2)使用和确定常数; (3)用它来表示算术平均速度. 7.尝试使用麦克斯韦速率分布函数来推断气体分子的最可能速率. 图中显示了8N个假设气体分子的速度分布(当v> 2 v0时,粒子数为零). 发现: (1)C; (2)比率介于v0和2v0之间的分子数目; (3)气体分子的平均速率.
本文来自电脑杂谈,转载请注明本文网址:
http://www.pc-fly.com/a/dianqi/article-233629-1.html
 捷西烤漆橱柜_捷西和欧牌橱柜哪个好_捷西橱柜烤漆
捷西烤漆橱柜_捷西和欧牌橱柜哪个好_捷西橱柜烤漆 热龙的热管家txt_火爆妖夫txtSina_凤舞江山热狼conc太恶魔txt
热龙的热管家txt_火爆妖夫txtSina_凤舞江山热狼conc太恶魔txt 台式计算机的固态硬盘安装方法和步骤教程
台式计算机的固态硬盘安装方法和步骤教程 美的空调显示屏E3故障的原因及解决方法-美的空调维修案例
美的空调显示屏E3故障的原因及解决方法-美的空调维修案例
否则后患无穷