(1)除去KNO3固体中混有的少量NaCl,所进行的实验操作
电脑杂谈 发布时间:2019-05-23 02:21:35 来源:网络整理
(1)除去KNO3固体中混有的少量NaCl,所进行的实验操作依次为_____、蒸发浓缩、冷却结晶、_________。
(2)除去KCl溶液中的K2SO4,依次加入的溶液为__________(填溶质的化学式)
(3)选择合适的操作方法,对下列物质进行分离提纯(用序号作答,如果有多步操作请注
意顺序蒸发浓缩冷却结晶。)

A.过滤 B.蒸发 C.分液 D.萃取
E.蒸馏 F.加热分解 G.渗析 H.重结晶
①分离油水混合物________;
②用自来水制取蒸馏水_________;

③除去氧化钙中的碳酸钙________;
④提纯Fe(OH)3胶体_______
⑤分离饱和食盐水和沙子________。
用无水乙醇配制质量浓度分别为20、50、100、150、200 μg/ml的大籽蒿精油溶液,配制同样质量浓度的vc溶液作为对照样品溶液。 ca10 (po4)6 f2 + 2oh- ③ k由于①-②=③k = ksp1/ksp2 = 6.8×10-37/1.0×10-60 = 6.8×10234. 沉淀的转化用1.0l的na2co3溶液将0.01 mol的baso4转化为baco3,问需要na2co3溶液的最低浓度为多少。习题“(14分)i.草酸晶体的组成可用h2c2o4·x h2o表示,为了测定x值,进行如下实验:(1) 称取wg草酸晶体,配成100.00 ml水溶液(2) 取25.00ml所配制的草酸溶液置于锥形瓶内,加入适量稀h2so4后,用浓度为a mol·l—1的kmno4溶液滴定至kmno4不再褪色为止,所发生的反应为:2 kmno4 + 5 h2c2o4 + 3 h2so4 = k2so4 + 10co2↑ + 2mnso4 + 8h2o试回答:①在滴定过程中若用去a mol·l—1的kmno4溶液v ml,则所配制的草酸溶液的物质的量浓度为____mol·l—1,由此可计算x的值是____。
(5)某同学用托盘天平称量镁粉25.2g(1g以下用游码),他把镁粉放在右盘,当天平平衡时,所称取的镁粉的实际质量是_____________。
答案及解析:
知识点:物质的分离、除杂和提纯
(1)溶解 过滤 (2) BaCl2、K2CO3、HCl (3)C E F G A

(4)10.6g (5)24.8g
【分析】
(1)硝酸钾的溶解度受温度影响大,而NaCl溶解度受温度影响不大;(2)根据硫酸根离子与钡离子结合生成硫酸钡沉淀分析;(3)①油与水混合,分层;②自来水中水的沸点较低;③碳酸钙加热分解为氧化钙和二氧化碳;④Fe(OH)3胶体粒子不能透过半透膜、溶液中的粒子可以透过半透膜;⑤沙子难溶于水;(4)配制480mL0.200 mol·L-l Na2CO3溶液,需用500mL的容量瓶;(5)根据托盘天平的平衡原理,“右+游=左”进行分析。
【详解】(1)硝酸钾的溶解度受温度影响大,而NaCl溶解度受温度影响不大,则溶解后、蒸发浓缩、冷却结晶、过滤可得到硝酸钾晶体;(2)硫酸根离子与钡离子结合生成沉淀,先加过量氯化钡将硫酸根离子转化为沉淀,再加碳酸钾除去过量的钡离子,最后加适量盐酸除去碳酸钾,所以依次加入的溶液为BaCl2、K2CO3、HCl;(3)①油与水混合,分层,用分液法分离,选C;②自来水中水的沸点较低,用蒸馏发制备蒸馏水,选E;③碳酸钙加热分解为氧化钙和二氧化碳,用加热分解的方法除去氧化钙中的碳酸钙,选F;④Fe(OH)3胶体粒子不能透过半透膜、溶液中的粒子可以透过半透膜,用渗析发提纯Fe(OH)3胶体,选G;⑤沙子难溶于水,用过滤法分离饱和食盐水和沙子,选A;(4)配制480mL0.200 mol·L-l Na2CO3溶液,需用500mL的容量瓶,需要Na2CO3的质量为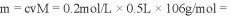 10.6g ;(5)用托盘天平称量镁粉25.2g,需用25g的砝码,若放颠倒,则镁粉的质量+游码=砝码质量,所称取的镁粉的实际质量是25-0.2=24.8g蒸发浓缩冷却结晶。
10.6g ;(5)用托盘天平称量镁粉25.2g,需用25g的砝码,若放颠倒,则镁粉的质量+游码=砝码质量,所称取的镁粉的实际质量是25-0.2=24.8g蒸发浓缩冷却结晶。
i、蒸发和结晶 蒸发是将溶液浓缩、溶剂气化或溶质以晶体析出的方法.结晶是溶质从溶液中析出晶体的过程,可以用来分离和提纯几种可溶性固体的混合物.结晶的原理是根据混合物中各成分在某种溶剂里的溶解度的不同,通过蒸发减少溶剂或降低温度使溶解度变小,从而使晶体析出.加热蒸发皿使溶液蒸发时、要用玻璃棒不断搅动溶液,防止由于局部温度过高,造成液滴飞溅.当蒸发皿中出现较多的固体时,即停止加热,例如用结晶的方法分离nacl和kno3混合物.。(4) 加入氨水,形成[ag(nh3)2]cl配合物,agcl的溶解度增大5.6 沉淀溶解平衡一、溶度积与溶解度二、沉淀溶解平衡的移动1.同离子效应与盐效应2. 酸度的影响3. 分步沉淀4. 沉淀的转化5. 沉淀的溶解一、溶度积与溶解度1. 溶度积常数ksp2. 溶度积规则3. 溶度积与溶解度的换算难溶物微溶物易溶物0.1/1000.01g/100g 水1. 溶度积常数ksp物质的溶解度只有大小之分,没有在水中绝对不溶解的物质。另外,的溶解能力远强于水,因此有一部分原来不能够被水溶解的物质会溶解到中来,因此溶剂萃取法得到的结果还包含水蒸气蒸馏法不能够得到的物质--这些物质主要是色酮、植物蜡、树脂和色素。
本文来自电脑杂谈,转载请注明本文网址:
http://www.pc-fly.com/a/dianqi/article-100668-1.html
-

-
 辛俊令
辛俊令改变不了了
-
 张偁
张偁我们坐实12海里要了里子
-
 50d8800tcl电视报价_tclle50d8800外接音箱_tcl50寸液晶电视价格
50d8800tcl电视报价_tclle50d8800外接音箱_tcl50寸液晶电视价格 什么是低级格式?如何对磁盘进行低级格式化
什么是低级格式?如何对磁盘进行低级格式化 江苏省小型冷风机销售电话
江苏省小型冷风机销售电话 Hard Disk Partition_DiskGenius v5.1.1.696官方中文版
Hard Disk Partition_DiskGenius v5.1.1.696官方中文版
美国需要慢慢习惯